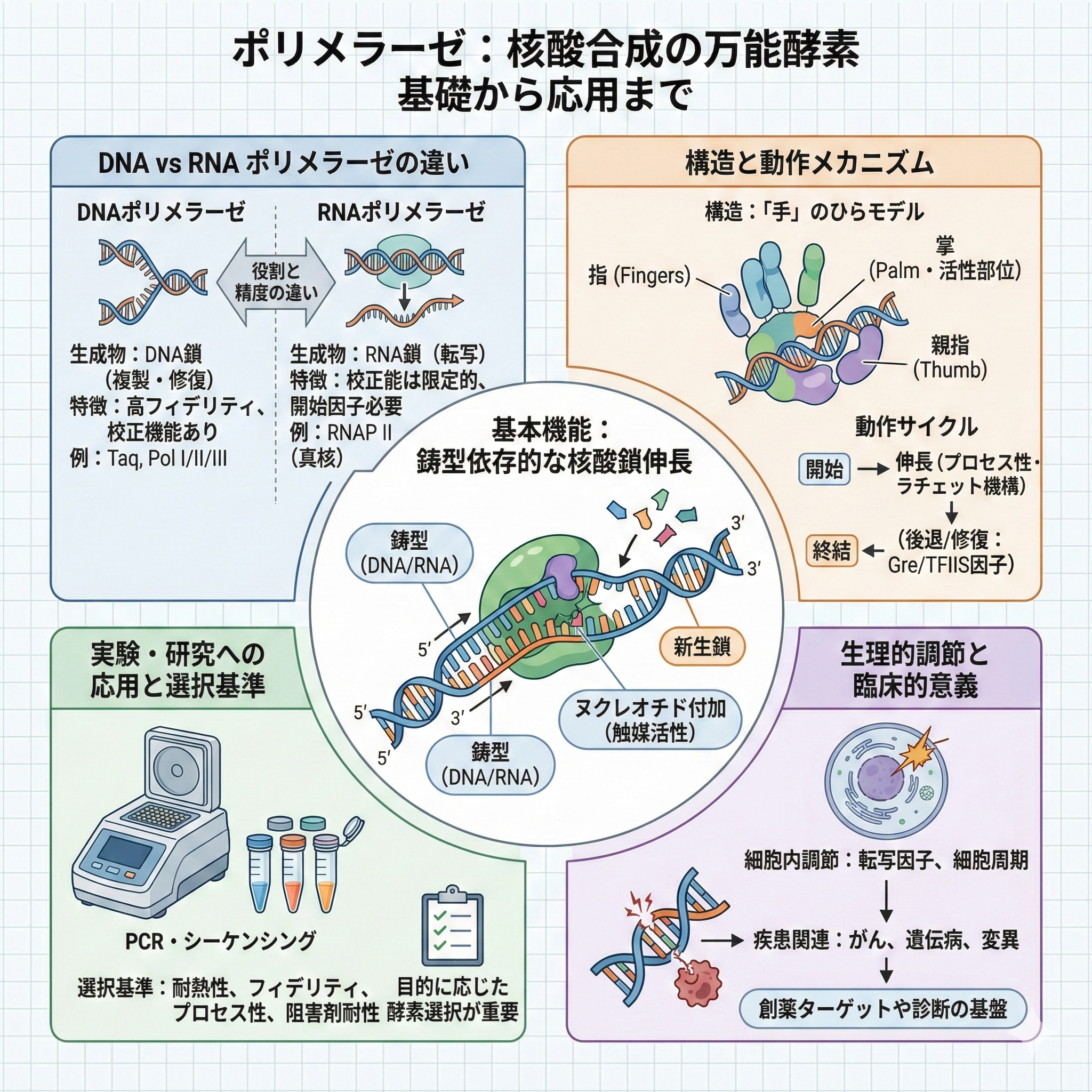
ポリメラーゼとは、核酸を鋳型として新しい核酸鎖を合成する酵素の総称です。[1]
この記事では「ポリメラーゼとは何か」という基本定義から、DNAとRNAを区別した機能の違い、主要な種類や構造、動作メカニズム、実験応用や臨床的な意味合いまでをコンパクトに整理して解説します。
5分で主要ポイントが掴めるように、図解や比較表、実験での選び方チェックリストも含めてまとめています。
ポリメラーゼに関連する解説記事
以下のポリメラーゼに関連するDAVIDIA collageの解説も合わせて読んで理解を深めましょう!
ポリメラーゼとは?5分で納得の基礎ガイド
ポリメラーゼは核酸を鋳型として新しい核酸鎖を合成する酵素の総称です。[1]
生体内ではDNA複製や転写、修復などに不可欠であり、分子生物学実験ではPCRやシーケンシングの中核として活用されます。[2][3]
この記事ではまず定義と語源、次にDNAとRNAポリメラーゼの違い、さらに構造や動作機構、実験応用までを順に解説します。
ポリメラーゼとは基本解説:語源・役割を簡単に
「ポリメラーゼ(polymerase)」という名前は『多くを結合する(重合する)酵素』という意味合いで用いられます。[1]
生化学的にはヌクレオチドを連結して長鎖の核酸ポリマーを形成する触媒活性を持つタンパク質群を指します。[1]
細胞では遺伝情報の正確な複製と表現に深く関わり、その種類や活性は細胞周期やストレス応答にも影響します。[4]
ポリメラーゼの定義──酵素・タンパク質として何をするか
ポリメラーゼは既存の核酸鎖を鋳型として相補的な塩基配列を持つ新生鎖を伸長させる酵素です。[1]
反応はヌクレオチド三リン酸が3’末端の水酸基に付加され、ピロリン酸が放出されることで進行します。[4][5]
生体内ではDNA複製、転写、修復やテロメア伸長など多様なプロセスに関与し、その機能は生命活動の基盤です。[1]
鋳型(DNA/RNA)依存性と合成の原理(触媒作用の基礎)
ポリメラーゼは鋳型依存性を持ち、鋳型がDNAかRNAかによってDNA依存性DNAポリメラーゼやDNA依存性RNAポリメラーゼなどに分類されます。[1]
酵素の活性部位はヌクレオチドの選択と結合を行い、正しい塩基対形成を触媒して鎖伸長を進めます。[5]
反応(ヌクレオチド付加)の触媒は「二金属イオン機構(two-metal-ion mechanism)」として広く整理されています。[5]
語源と発見史:誰がいつ“polymerase”を見つけたか
ポリメラーゼ活性の発見は20世紀半ばに大きく進み、特に1950年代にArthur Kornbergらが大腸菌抽出物からDNA合成活性を示す酵素(後のDNA polymerase I)を同定した研究が転機となりました。[6][7]
その後、RNAポリメラーゼや各種DNAポリメラーゼの同定・分類が進み、構造解析(X線結晶構造解析やクライオEM)により現在の機能理解が確立していきました。[8][9]
DNAポリメラーゼとRNAポリメラーゼの違いを図解で理解
DNAポリメラーゼとRNAポリメラーゼはどちらも核酸合成を行いますが、鋳型・生成物・校正機構・役割が異なります。[1]
ここでは主要な違いを表で比較し、その後に個別の機能と生物学的意義を説明します。
研究や実験で適切な酵素を選ぶ際には、鋳型依存性、フィデリティ、耐熱性などを基準に判断します。
| 項目 | DNAポリメラーゼ | RNAポリメラーゼ |
|---|---|---|
| 鋳型 | DNA | DNA |
| 生成物 | DNA鎖 | RNA鎖(mRNA、rRNAなど) |
| 主要役割 | 複製・修復 | 転写(遺伝情報の読み取り) |
| 校正機構 | エキソヌクレアーゼ活性を持つものが多い | 一般に校正能力は低いが因子で補助される場合がある |
| 例 | Pol I/II/III、Taqなど | RNAポリメラーゼII(真核)、RNAP(原核) |
DNAポリメラーゼの働き:DNA複製での役割と依存性
DNAポリメラーゼは複製フォークで親鎖を鋳型に新しい鎖を合成します。[1]
プライマーの3’末端(3′-OH)を必要とすることが基本で、複製ではプライマー合成酵素(プライマーゼ)やヘリカーゼ、トポイソメラーゼなどと協調して働きます。[4]
高いフィデリティを保つために校正機能(3’→5’エキソヌクレアーゼ)やスライディングクランプなどの補因子を利用する点が特徴です。[1]
RNAポリメラーゼとは何か:転写とmRNA合成の基本
RNAポリメラーゼはDNAの特定領域(遺伝子)を鋳型にしてRNAを合成します。[1]
プロモーター認識や転写因子の結合により開始点が決定され、開始後は伸長複合体が進むことでmRNA前駆体やrRNA、tRNAが合成されます。[4]
なお、DNAポリメラーゼと異なり、RNAポリメラーゼは一般にプライマーなしでde novoに転写を開始できます。[10]
フィデリティと校正機構(エキソヌクレアーゼ活性など)
フィデリティは誤った塩基の挿入頻度に関わる性質で、多くのDNAポリメラーゼは3’→5’エキソヌクレアーゼ活性を持ち、誤挿入を除去して高精度な複製を実現します。[1]
RNAポリメラーゼは一般にDNAポリメラーゼほどの校正能は高くありませんが、バックトラックと切断(transcript cleavage)を介する誤り是正が知られ、原核ではGreA/GreB、真核のPol IIではTFIISが回復を助けます。[11][12][13]
フィデリティは生物種や酵素の種類で大きく異なります。[1]
原核生物 vs 真核生物の違い(大腸菌・古細菌・Pol I/II/III)
原核生物では比較的単純なRNAポリメラーゼ複合体とDNA複製酵素群が働きます。[4]
真核生物ではPol I/II/IIIなど複数のRNAポリメラーゼが存在し、多様なDNAポリメラーゼとともに核内で高度に制御されたプロセスを行います。[1]
古細菌は真核に類似する特性を持つ要素があり、進化的知見を与えます。[14]
ポリメラーゼの種類と構造:複合体・結晶構造から見る機能
ポリメラーゼ群は単量体から多サブユニットの複合体まで多様な形態を取り、結晶構造やクライオEM解析により活性部位やサブユニット間相互作用が明らかになっています。[9]
構造情報は基質認識、校正機構、プロセス性(連続伸長能力)や耐熱性といった機能と密接に関連しており、工学的改変や酵素選択の基礎になります。[5][9]
代表的なポリメラーゼ群(Taq、DNAポリメラーゼ、RNAポリメラーゼほか)
研究や応用でよく知られる例として、PCRで使われる耐熱性のTaqポリメラーゼ、真核細胞で複製に関与するDNAポリメラーゼδやε、転写を担うRNAポリメラーゼIIなどがあります。[2][1]
さらに、損傷部位を乗り越えるトランスレッショナルポリメラーゼや、ウイルス由来ポリメラーゼなど多様なグループが存在します。[1]
複合体とサブユニット構成:protein/polymeraseとしての立体配置
多くのポリメラーゼは複数のサブユニットが協調して働き、触媒サブユニットに加え、プロセス性を高める因子や補助サブユニットを持ちます。[1]
立体配置は鋳型結合部位やヌクレオチド取り込みチャネルを形成し、動的な構造変化が触媒サイクルを推進します。[9]
サブユニット間相互作用は機能調節の要です。[9]
構造と活性部位:ラチェット機構・チャネル・触媒残基
多くのポリメラーゼは「手」のようなドメイン配置(掌・指・親指など)を持ち、ヌクレオチドの取り込みや塩基対形成を制御します。[5]
触媒は金属イオンを介した反応として説明され、構造研究により活性部位の配置や反応過程が整理されています。[5]
結晶構造・クライオEMが解明した知見と耐熱性・フィデリティの関係
結晶構造やクライオEM解析により、RNAポリメラーゼIIの「クランプ」などの可動要素や、転写バブル・DNA/RNAハイブリッドの配置が詳細に示されました。[9][15]
こうした構造知見は、機能(伸長・転位・停止・校正)理解や、酵素工学(高耐熱性・高フィデリティ改変)の基盤として活用されています。[5][9]
動作メカニズム:開始・伸長・後退(ラチェット・休止・ヘアピン)
ポリメラーゼの動作は一般に開始、伸長、終結のサイクルを持ちます。[1]
転写の際には鋳型上の二次構造や障害物によって後退(バックトラック)や休止が生じ、専用の因子がそれらを処理します。[11][12]
これらの動的挙動は遺伝情報の正確な伝達と調節に影響します。[13]
転写開始から伸長へ:プロモーターと転写因子の結合・役割
転写開始ではRNAポリメラーゼがプロモーター配列を認識し、転写因子やコア複合体の協調で開始複合体が形成されます。[4]
開始複合体から安定な伸長複合体へ移行する過程や、構造要素(クランプなど)の役割は構造生物学的にも整理されています。[9]
伸長と後退(バックトラック)の仕組みとGre因子による処理
伸長中にミスマッチや障害で後退(バックトラック)すると、3’末端が活性部位から外れて伸長が停止します。[12]
原核生物ではGreA/GreB、真核生物ではTFIISがRNA切断を促進し、正しい3’末端を再構築して伸長を再開させます。[11][13]
これは転写品質管理の重要な機構です。[13]
ヘアピンや一本鎖構造が転写/複製に与える影響
鋳型上の二次構造(例:ヘアピンなど)はポリメラーゼの進行を阻害し、転写停止や複製ストレスを引き起こすことがあります。[1]
細胞はヘリカーゼやRNA結合タンパク質、修復機構を使ってこれらを解消し、遺伝情報の安定性を保っています。[1]
終結・切断・処理:mRNA生成と後処理の概念
転写の終結は種によって異なり、ポリメラーゼが特定配列や因子により停止して切断が行われます。[4]
真核生物のmRNAではポリA付加、5’キャップ、スプライシングなどの後処理が行われ、成熟mRNAが輸送・翻訳に回されます。[4]
研究・解析手法と実験応用:PCR法から構造解析まで
ポリメラーゼは実験応用の中心で、PCRやqPCR、シーケンシング、クローニング、診断検査などで不可欠です。[2]
研究では酵素の選択が結果の精度や感度に直結するため、耐熱性、フィデリティ、プロセス性、エラー特性などを考慮します。
また構造解析や変異解析を通じて新規酵素や改変酵素の開発が進められています。[5][9]
PCRに使われるポリメラーゼと技術(Taq、耐熱性・増幅の原理)
PCRでは耐熱性を持つポリメラーゼ(代表例はTaq)が使われ、熱変性、プライマーアニーリング、伸長のサイクルを繰り返すことで指数的増幅を実現します。[2]
耐熱性により高温での鋳型変性が可能となり、増幅特異性が向上します。[2]
高フィデリティが必要な場合は校正活性(proofreading)を持つ酵素が選ばれます。[1]
増幅・シーケンシング・診断応用でのポリメラーゼの選び方
用途に応じて酵素を選ぶ基準は、耐熱性、フィデリティ、プロセス性、阻害物質耐性などです。
診断用途では感度と特異性が重要で、臨床サンプル中の阻害因子への耐性も考慮します。[2]
シーケンシングでは正確な複製が重要なため高フィデリティ酵素が好まれます。[1]
酵素特性の解析(活性、特異性、塩基配列依存性、フィデリティ測定)
酵素特性の評価には基質速度論、温度特性、塩濃度やpH依存性の測定、ミスマッチに対する取り込み率、エラー頻度の解析などが用いられます。[1]
フィデリティ測定では既知配列を用いた変異解析や、次世代シーケンスを活用した検出が一般的です。
結晶構造・解析手法と参考文献・リーディングリスト
ポリメラーゼの構造解析はX線結晶構造解析やクライオ電子顕微鏡(クライオEM)により進展しました。[9]
代表的なレビューや原著論文、Protein Data Bankの構造エントリーを参照することで詳細な立体情報が得られます。[15]
学術レビューや教科書、オンラインデータベースを組み合わせて学ぶことを勧めます。
生理的調節と臨床/研究分野への影響
ポリメラーゼの活性は転写因子、修飾、複合体形成、細胞周期シグナルなどで厳密に調節されています。[1]
異常や変異は複製誤差の増加、癌や遺伝性疾患への寄与、治療薬耐性などに関係します。[1]
研究分野ではポリメラーゼを標的とした薬剤開発や診断法の基盤研究が進められています。
細胞内での調節機構:転写因子・プロモーター結合・因子による制御
転写はプロモーター配列と結合する転写因子やクロマチン状態に強く依存します。[4]
転写因子はポリメラーゼ複合体の呼び込みや活性化、抑制を行い、エピジェネティック修飾やリモデリング複合体はアクセス性を変化させます。[4]
これらの調節は細胞応答や発生過程で重要な役割を果たします。
DNA修復・損傷応答におけるポリメラーゼの役割と関連疾患
DNA損傷応答では特定のポリメラーゼが損傷部位の合成やトランスレッショナル合成を担当し、エラーを許容してでも複製を続行することで細胞生存を助けます。[1]
これらの活性の異常は腫瘍形成や遺伝性疾患につながる場合があり、修復系とポリメラーゼの関係は臨床的にも重要です。[1]
変異・活性変化がもたらす生物学的影響と応用上の課題
ポリメラーゼの変異はフィデリティ低下、プロセス性変化、阻害剤耐性などを引き起こし、ゲノム不安定性や治療抵抗の基礎となることがあります。[1]
応用面では酵素の不安定性やサンプル中の阻害物質、オフターゲット合成が課題であり、それらを考慮した設計と品質管理が必要です。
今後の研究課題と分野別の応用展望(バイオ・診断・技術開発)
将来の研究課題には高精度で耐環境性の高いポリメラーゼの設計、損傷DNAの複製機構の解明、ポリメラーゼ制御を標的とした新規治療法の開発などがあります。[5]
応用面では迅速診断、環境サンプリング、合成生物学での技術開発など多岐にわたる展望があります。
まとめ:ポリメラーゼとは何かを5分で振り返るチェックリスト
ポリメラーゼは核酸合成酵素であり、DNA複製や転写、修復に中心的な役割を果たします。[1]
DNAとRNAポリメラーゼは鋳型や生成物、校正能が異なり、用途に応じた選択が重要です。[4]
実験や臨床応用では耐熱性、フィデリティ、プロセス性を基準に酵素を選び、構造情報は酵素設計に有用です。[2][5][9]
要点チェック(定義・DNA/RNAの違い・主要な応用)
主な要点は次の通りです。
ポリメラーゼは核酸を伸長する酵素であること。
DNAポリメラーゼは複製と修復、RNAポリメラーゼは転写を担うこと。
PCRやシーケンスなど実験応用では酵素特性の適切な選択が成功の鍵となること。
さらに学ぶための参考文献・オンラインリソース(解説・研究論文)
基礎学習には分子生物学や生化学の教科書、レビュー論文が有用です。
構造情報はProtein Data Bank、レビューはNCBI Bookshelf(The Cell / Molecular Biology of the Cell)や総説論文が参考になります。[4][15]
実験プロトコルは論文・プロトコル集・メーカーのアプリケーションノートも役立ちます。
参考文献
- Alberts B, et al. Molecular Biology of the Cell (NCBI Bookshelf): DNA Replication Mechanisms.
- Saiki RK, et al. Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science. 1988.
- RCSB PDB: 1Y1W Complete RNA Polymerase II elongation complex(構造エントリー).
- The Cell (NCBI Bookshelf): DNA Replication.
- Pata JD. Nucleic Acid Polymerases: The Two-Metal-Ion Mechanism and Beyond. 2022. (PMC)
- Lehman IR. Discovery of DNA Polymerase. J Biol Chem. 2003.
- Friedberg EC. The eureka enzyme: the discovery of DNA polymerase. 2006.
- Cramer P, et al. RNA polymerase II at 2.8 angstrom resolution. Science. 2001. (PubMed)
- Schier AC, Taatjes DJ. Structure and mechanism of the RNA polymerase II transcription machinery. Genes & Development. 2020.
- The Cell (NCBI Bookshelf): Transcription in Prokaryotes(RNAポリメラーゼはプライマー不要でde novo開始).
- Laptenko O, Borukhov S. Transcript cleavage factors GreA and GreB act as transient catalytic components of RNA polymerase. 2003. (PMC)
- Abdelkareem M, et al. Structural Basis of Transcription: RNA Polymerase proofreading/backtracking and Gre factors(総説). 2019. (PMC)
- Xu L, et al. RNA polymerase II transcriptional fidelity control and its functional implications. 2015. (PMC)
- Forterre P. Origin and Evolution of DNA and DNA Replication Machineries(DNAポリメラーゼのプライマー要求性など). 2013. (NCBI Bookshelf)
- RCSB PDB: 1Y1W(Pol II 伸長複合体の構造情報).